Le Savon : Découvrez comment et pourquoi le savon lave !
Savon Noir, savon d’Alep, savons liquides… Ils font partie intégrante de notre quotidien et nous connaissons tous.tes ces produits d’hygiènes indispensables qui nous permettent d’être tout.e propre en toutes circonstances. Mais est-ce que vous vous êtes déjà demandé pourquoi le savon lave ? ?
Après tout, quand on y pense, pour nous, le savon il fait des bulles, il mousse, il sent bon, c’est normal qu’il nettoie, mais, en vrai, comment ça se fait ? ?
1/ Qu’est-ce qu’un savon ?
On va vous faire un petit cours de chimie rapide et simple et, après ça, le savon n’aura plus de secret pour vous ! Comme tout vrai cours qui se respecte, on commence toujours par une petite définition du sujet : le savon ?.
Un savon est un tensioactif anionique, connu sous le terme de sel d’acides gras. Il fait partie de la même famille qu’un dérivé sulfaté qu’on retrouve dans un gel douche ou un shampoing (les sulfates en moins ?). En fait, le savon est une molécule amphiphile. Késako ? Pas de panique, on vous explique. On peut visualiser ça comme un têtard avec : la tête hydrophile (= qui est attirée par l’eau) et la queue hydrophobe (= qui, au contraire, n’aime pas l’eau mais plutôt le gras). Grâce à ses différentes affinités, cette molécule va agir sur la tension superficielle de l’eau. Ça peut paraitre un peu barbare dit comme ça, mais pas de panique on vous explique tout ! ?
2/ Zoom sur la tension superficielle de l’eau ?
La tension superficielle de l’eau est une sorte de compétition entre plusieurs molécules. D’un côté, les molécules naturellement présentes dans l’eau et attirées entre elles. De l’autre, les molécules d’eau présentes sur une surface qui sont attirées vers l’intérieur (par exemple, votre peau). Ainsi, cette tension se caractérise par la formation de gouttelettes d’eau sur une surface, qui vont diminuer le pouvoir “mouillant” de l’eau sur votre peau. Ce phénomène empêche l’eau de s’étaler partout et le processus de nettoyage va être limité.

En bref, l’eau toute seule ne mouille pas tout notre corps ! Faites le test, passez votre main sous l’eau avec du gras dessus. L’eau ne va pas vous mouiller partout ! Vous aurez beau frotter, vous ne serez pas beaucoup lavé.e ?. Eh oui, l’eau et l’huile, vous le savez, ça ne se mélange pas !
3/ Les savons : comment fonctionnent-t-ils ?
Le savon, en tant que tensioactif, va réduire cette tension à la surface de l’eau. Celui-ci va permettre de mieux “mouiller” et donc nettoyer notre peau grâce à sa propriété amphiphile.
Dans l’eau, le savon se présente sous forme de micelles. C’est une sorte de gouttelette avec les têtes hydrophiles à l’extérieur de la goutte et les queues hydrophobes à l’intérieur.
Alors, quand la micelle de savon va rencontrer une partie grasse à nettoyer ?, la gouttelette va s’ouvrir. Ensuite, les parties hydrophobes (qui aiment le gras) vont être attirées par cette saleté. Enfin, elles vont s’y accrocher pour la renfermer dans la micelle de savon. Pour finir, les eaux de rinçage vont emporter la gouttelette de savon contenant la saleté. En effet, les têtes hydrophiles de la micelle vont, elles, s’accrocher à l’eau et, hop, tout le monde au fond du siphon ! ?
En bonus : un petit schéma simple et efficace qui résume ce cours de sciences ! ?
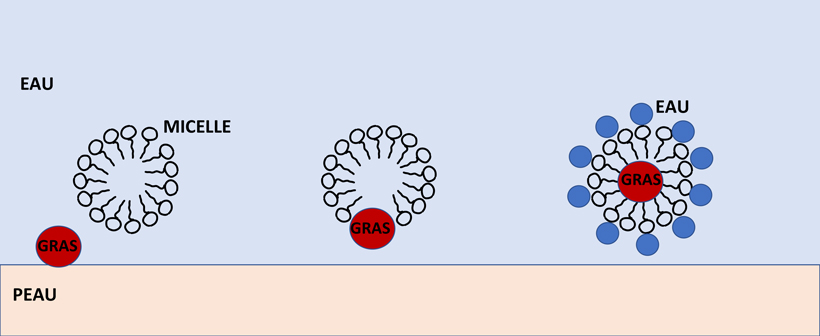
? Petit point sur la mousse : Elle ne participe pas au nettoyage, donc un savon qui mousse peu ne veut pas forcément dire savon qui lave moins ?. C’est juste le résultat de l’agitation de l’eau qui forme des bulles d’air, enveloppées par du savon.
? Pour devenir expert.e sur l’univers du savon : Les différences entre le savon de Marseille et le savon saponifié à froid
Et voilà, vous savez tout sur le mode d’action du savon ! Il est d’ailleurs le même pour le shampoing ou le liquide vaisselle ainsi que les autres produits nettoyants contenant des tensioactifs ! Intéressant, n’est-ce pas ? Qui a dit que la chimie ce n’était pas cool ? ?
Apolline de la Biotyfull Team



